01.08.2019
Vector Flow Mapping – это технология визуализации кровотока и измерения его параметров в сердце и сосудах. Понимание гемодинамики должно улучшить качество диагностики, точность прогноза и оценку эффекта лечения при наличии патологии сердца.
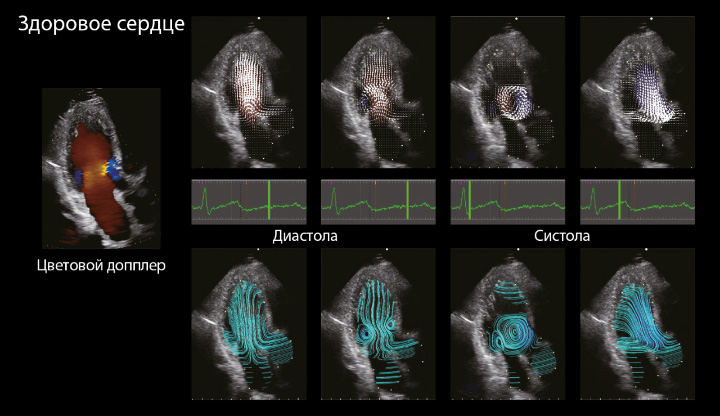
Иллюстрация работы технологии на примере здорового сердца
Автор: Кеиичи Итатани (Keiichi Itatani), отделение сердечно-сосудистой хирургии, лаборатория исследования сердечно-сосудистой визуализации, взрослый центр врождённых сердечных заболеваний, Университет Медицины Префектуры Киото (Kyoto Prefectural University of Medicine)
Векторное картирование позволяет на основе B-режима и цветового допплера представить кровоток в сердце и сосудах в виде векторов, отражающих направление и скорость потоков1 (см. рисунок 1).
Рисунок 1. Векторное картирование кровотока
Обычный допплеровский режим предоставляет информацию о скорости потока по направлению луча (продольная составляющая вектора), но не может использоваться для измерения скоростей по другим направлениям. Для получения ортогональной (или поперечной) составляющей вектора и реализации функции VFM используется уравнение неразрывности потока в двухмерном срезе. Каждый вектор вычисляется для элементарного объёма малого размера с малыми потоками.
Рисунок 2. Вычисление скорости по VFM
Погрешность измерения скорости с помощью VFM была измерена на фантоме и составила не более 10% от значения, полученного в режиме цветового допплеровского картирования2. В технологии реализована оценка точности измерения для выявления ошибок отображения векторной картины3.
Рассмотрим подробнее процесс вычисления поперечной компоненты вектора. В начале эхокардиографическое изображение разбивается на элементарные объёмы: представляется, что лучи, выходящие из датчика, пересекаются с некоторыми виртуальными концентрическими окружностями (см. рисунок 3). Для каждой клетки применяется уравнение неразрывности: приток и отток – с учётом продольных допплеровских составляющих – для каждой клетки равны. Первое значение скорости получается из скорости движения стенки сердца или сосуда в соседней клетке, вычисленной с помощью метода слежения за спеклами («speckle tracking») (см. рисунок 3 (1)). Затем, как показано на рисунке 3 (2), измеряются скорости притока и оттока для каждой клетки. Теперь, когда имеются данные о скоростях с трёх сторон, вычисляется скорость оставшегося поперечного направления.
Скорость для одного из двух ортогональных направлений в последующих клетках получается таким же образом (см. рисунок 3 (3)). В итоге, если могут быть вычислены значения для каждого элементарного объёма, получается полная картина распределения векторов кровотока.
Рисунок 3: Вычисление поперечных составляющих векторов с помощью принципа неразрывности потока
При подготовке к исследованию в режиме векторного картирования кровотока необходимо руководствоваться следующими правилами:
Рисунок 4. Выставление области интереса согласно принципам VFM
Автор: Сеиджи Ойама (Seiji Oyama), отдел здравоохранения Hitachi, Ltd.
Чтобы сэкономить время и упросить процедуру оконтуривания области интереса на трёхкамерном срезе, предложено устанавливать всего шесть точек, как указано на рисунке 5: три точки на кольце митрального клапана, одна точка на верхушке и по одной точке на приток и отток. После этого автоматизированный алгоритм оконтуривает остальные участки эндокарда левого желудочка и выставляет небольшие запасы в участках притока и оттока в каждом кадре. Автоматизация оконтуривания также работает на двухкамерных и четырёхкамерных срезах, в таком случае необходимо выставлять всего четыре точки: две – на кольцо митрального клапана, одну – на верхушку и одну – на приток.
Рисунок 5: Опорные точки в автоматическом режиме (сверху) и выставленные точки слежения (снизу)
Эта функция снижает нагрузку на врача, избавляя его от десяти или более дополнительных манипуляций, необходимых при работе вручную. При использовании автоматизации, выигрыш во времени подготовки к исследованию может составить до 70%.
Рисунок 6: Время необходимое для подготовки исследования
Автор: Кеиичи Итатани (Keiichi Itatani), отделение сердечно-сосудистой хирургии, лаборатория исследования сердечно-сосудистой визуализации, взрослый центр врождённых сердечных заболеваний, Университет Медицины Префектуры Киото (Kyoto Prefectural University of Medicine)
Под интенсивностью потока понимается направление и интенсивность вращающего движения векторов в центре турбулентности. Векторы скорости кровотока имеют продольные и поперечные составляющие, величины которых со временем изменяются по отношению к продольному и поперечному направлениям. К примеру, чтобы рассчитать интенсивность левостороннего потока, мы используем следующую формулу:
Интенсивность = (Поперечный прирост/убывание продольной скорости потока) – (Продольный прирост/убывание поперечной скорости потока)
Положительное значение означает возникновение интенсивного левостороннего потока (обозначается красным цветом), а отрицательное значение означает возникновение интенсивного правостороннего потока (обозначается синим цветом) (см. рисунок 7).
Рисунок 7. Картирование интенсивностей потока
Понятие «Циркуляция» отражает направление и интенсивность вращающего движения в пределах замкнутой области. Значение вычисляется путём суммирования всех скоростных компонент потока, входящих в область. Такая сумма теоретически соответствует сумме интенсивностей потоков в той же области.
Автор: Кеиичи Итатани (Keiichi Itatani), отделение сердечно-сосудистой хирургии, лаборатория исследования сердечно-сосудистой визуализации, взрослый центр врождённых сердечных заболеваний, Университет Медицины Префектуры Киото (Kyoto Prefectural University of Medicine)
Кровь является вязкой и из-за трения её элементов в турбулентных потоках выделятся тепловая энергия. Расход энергии в кровотоке принимается за энергию такого тепла1. Степень расхода в турбулентных потоках высчитывается по разнице направлений векторов: расход энергии больше в участках с частыми и значительными сменами направлений соседних векторов и меньше в ламинарных потоках, больших организованных турбулентных потоках или неподвижных участках (см. рисунок 8).
В клинической практике большой расход энергии возникает в стенозированных участках сосудистых анастомозов или при стенозах клапанов сердца. К примеру, турбулентный поток, возникший вследствие клапанной регургитации, вызывает сильное возмущение векторов и, как следствие, высокий расход энергии.
Рисунок 8. Расход энергии в кровотоке
Автор: Томохико Танака (Tomohiko Tanaka), центральная исследовательская лаборатория Hitachi, Ltd.
При визуализации относительного давления (Relative Pressure Imaging или RPI) оценивается распределение скоростей в одном срезе. Для вычислений используется уравнение Навье-Стокса для несжимаемых жидкостей4.
На рисунке 9 показаны примеры такой визуализации. Здесь синим цветом обозначено низкое давление, а красным – высокое. Посредине среза установлена референтная точка. На рисунке 9 (а) показано, что в раннюю диастолу давление в верхушке левого желудочка сердца меньше, чем на митральном клапане – происходит наполнение. На рисунке 9 (б) показано формирование турбулентного потока в центре левого желудочка, происходящее с конца диастолы и до изоволюмического сокращения: давление в этом потоке снижается.
(a) Ранняя диастола
(b) Период с конца диастолы до изоволюмического сокращения
Рисунок 9. Визуализация относительного давления
Точность оценки относительного давления была подтверждена с помощью эксперимента на фантоме левого желудочка, в котором были установлены два датчика давления. На рисунке 10 (а) приведена диаграмма экспериментальной установки, а на рисунке 10 (б) представлена её фотография. Мы сравнили результаты исследования RPI с показаниями датчиков давления и величины оказались сопоставимы4. Однако, в период наполнения градиенты давлений у верхушки и в приносящем тракте были занижены примерно на 30%. Мы считаем, что в будущем точность может быть улучшена при увеличении частоты кадров. Дело в том, что при измерениях давления в цветовом M-режиме (CMM) с высоким временным разрешением как раз наблюдается зависимость результатов от частоты кадров (см. рисунок 11).
(а)
(б)
Рисунок 10. Экспериментальная установка
Рисунок 11. Зависимость результатов измерения давления от частоты кадров
Кеиичи Итатани (Keiichi Itatani), отделение сердечно-сосудистой хирургии, лаборатория исследования сердечно-сосудистой визуализации, взрослый центр врождённых сердечных заболеваний, Университет Медицины Префектуры Киото (Kyoto Prefectural University of Medicine)
Сеиджи Ойама (Seiji Oyama), отдел здравоохранения Hitachi, Ltd.
Томохико Танака (Tomohiko Tanaka), центральная исследовательская лаборатория Hitachi, Ltd.
Сатоши Накатани (Satoshi Nakatani), отделение функциональной диагностический науки, отдел медицинских технологий и наук, магистратура медицины в университете Осаки (Osaka University)
Уважаемые посетители!
Пожалуйста, при работе с нашим сайтом просим Вас учитывать приведенные ниже условия:
Если у Вас возникли вопросы, необходима консультация или Вы хотели бы получить дополнительную информацию, пожалуйста, просим обращаться к нам или к нашим дистрибьюторам!
Также можете ознакомиться с условиями использования информации, предоставленной на сайте и с политикой защиты персональных данных. Сайт использует Cookies (подробнее).